Exercice 1 : Lire une température

a. Quelle est la valeur d’une division sur chaque thermomètre ?
b. Quelles sont les températures indiquées ?
Exercice 2 : Choisir la bonne courbe

Quelle est la courbe qui représente les variations de température en fonction du temps, lors du chauffage del’eau pure sous la pression atmosphérique normale ?Justifie ta réponse.
Exercice 3 :
Lors de l’ étude de l’ ébullition de l’ eau, Mathias a tracé la courbe ci- dessous.

a. Quellegrandeur a-t-il porté sur l’axe des ordonnées ? Quelle est l’échelle choisie ?
b. Quelle grandeur a-t-il porté sur l’axe des abscisses ? Quelle est l’échelle choisie ?
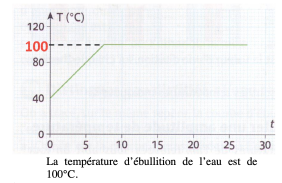
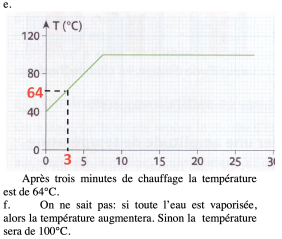
c. Quelle est la température d’ébullition de l’eau ?
d. A quel instant l’eau a-t-elle commencé à bouillir ?
e. Quelle était la température de l’eau après trois minutes de chauffage ?
f. Peut-on prévoir la température à l’instant t=30 min ? Justifie ta réponse.
Exercice 4 : Graphique d’un changement
a. On place de l’éther pur (un liquide incolore autre que l’ eau) dans un becher que l’on place sur une plaque chauffante. Toutes les 5 minutes on note la température.
On place ces mesures dans un tableau.
Tracez le graphique de la température en fonction du temps sur votre cahier :

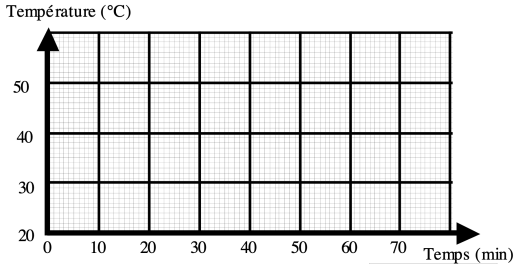
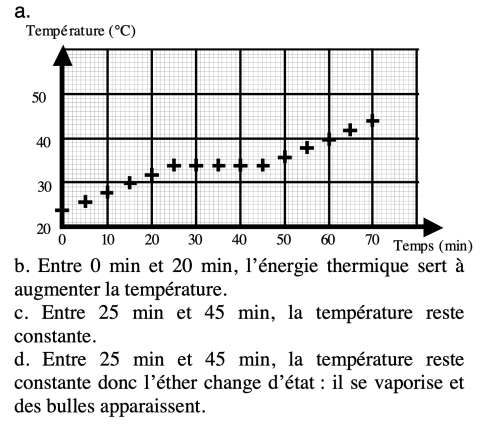
b. Quel est l’effet sur le liquide de la chaleur transmise par l’appareil de chauffage entre 0 min et 20 min ?
c. Entre 25 min et 45 min, comment varie la température ?
d. D’ après le graphique ou les mesures, que voit-on dans le liquide contenu dans le verre entre 25 min et 45 min (justifiez).
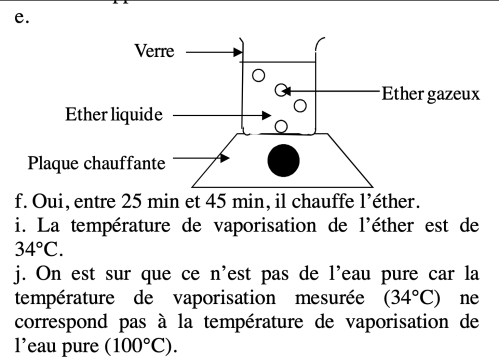
e. Faites le schéma de l’expérience entre 25 min et 45 min sans oublier les légendes (attention : le liquide de l’expérience n’est pas de l’eau mais de l’éther).
f. Entre 25 min et 45 min, l’appareil de chauffage chauffe-t-il l’éther ?
i. D’après le graphique ou les mesures, quelle est la température de vaporisation de l’éther ?
j. D’après le graphique ou les mesures, pourquoi est-on sûr que ce n’est pas de l’eau pure dont on a mesuré la température ?
Exercice 5 : Utiliser un tableau de donnée
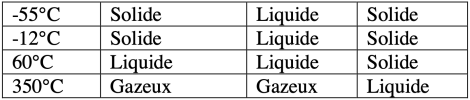
On désire connaître l’état physique de quelques corps purs pris à différentes températures. On dispose pour cela des données suivantes :
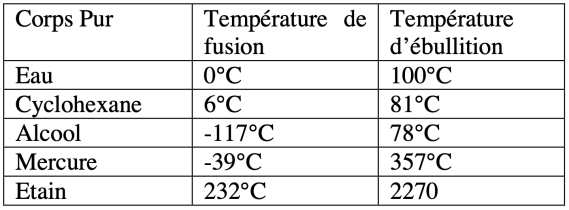
Indique, dans un tableau l'état physique du cyclohexane, de l’alcool et de l’étain aux températures suivantes : -55°C, -12°C, 60°C, 350°C.
Exercice 6 : le dioxygène
La température d’ébullition du dioxygène est de -183°C.
a. Dans quel état le trouve-t-on naturellement ?
b. A partir de quelle température le trouve-t-on à l’état liquide ?
c. Le dioxygène se trouve à l’état liquide dans certaines bouteilles. Comment est-ce possible ?
Correction
Exercice 1 : Lire une température

Exercice 2 : Choisir la bonne courbe
La courbe (a) représente les variations de température en fonction du temps, lors du chauffage de l’eau pure sous la pression atmosphérique normale car le palier a lieu pour une température de 100°C.
Exercice 3 :

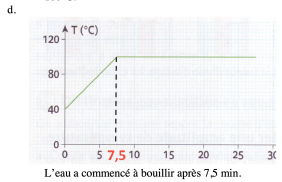
Exercice 4 : Graphique d’un changement
Exercice 5 : Utiliser un tableau de donnée
![]()
Exercice 6 : le dioxygène
a. On le trouve à naturellement l’état gazeux
b. On le trouve à l’état liquide pour des
températures inférieures à -183°C
c. Il est compressé : à une pression plus élevée, la température d’ébullition est moins faible.