Comment préparer une semoule au chocolat :
Réaliser une recette de cuisine met souvent en jeu des notions de Physique-Chimie.
Document 1
Ingrédients :
60 g de semoule de blé fine
50 g de chocolat pâtissier
12 g de sucre
50 cL de lait

5 ème
Chimie en cuisine
Chapitre 2
Comment préparer une semoule au chocolat :
Réaliser une recette de cuisine met souvent en jeu des notions de Physique-Chimie.
Document 1
Ingrédients :
60 g de semoule de blé fine
50 g de chocolat pâtissier
12 g de sucre
50 cL de lait


Document 2 :
Recette :
Étape 1 : Faire fondre le chocolat au bain-marie et mettre de côté.
Étape 2 : Mettre le lait et le sucre à chauffer à feu fort dans une casserole. Remuer régulièrement jusqu'à la première ébullition.
Étape 3 : Baisser le feu et verser alors le chocolat fondu dans le lait. Bien mélanger jusqu'à ce que l'on ne puisse plus distinguer les divers ingrédients.
Étape 4 : Ajouter immédiatement la semoule et continuer la cuisson pendant 3 à 4 minutes à feu moyen, en remuant puis laisser refroidir.
Document 3 :
Le bain-marie :
Le récipient contenant les ingrédients est posé dans une casserole dans laquelle on fait bouillir de l'eau.

Questions :
1-1 Dessiner un diagramme avec les changements d'état évoqués dans les doc. 2 et 3.
1-2 : Lorsqu’on verse le sucre dans le lait et que l'on mélange, le sucre semble disparaître. Expliquer en utilisant des termes scientifiques.
1-3 : Un volume de 50 cL de lait a une masse de 515g. Calculer la masse de lait sucré obtenue lors de l'étape 2 de la préparation (doc. 2 ).
1-4 : Exercices :

Le bain marie :
Le bain marie est une technique de chauffage qui permet de faire fondre le chocolat lentement et sans dépasser une certaine température.
2-1 : Dessine le matériel utilisé en cuisine
2-2 Hypothése : Expliquez pourquoi nous utilisons cette méthode pour faire fondre le chocolat.
2-3 On réalise l'expéreince, chématiser la avec le materiel de chimie.
2-4 Expérience : Pour vérifier votre hypothése, vous allez chauffer 200 ml d'eau et relever la tempéature de l'eau toutes les minutes pendant 10 mn.
Adaptation :
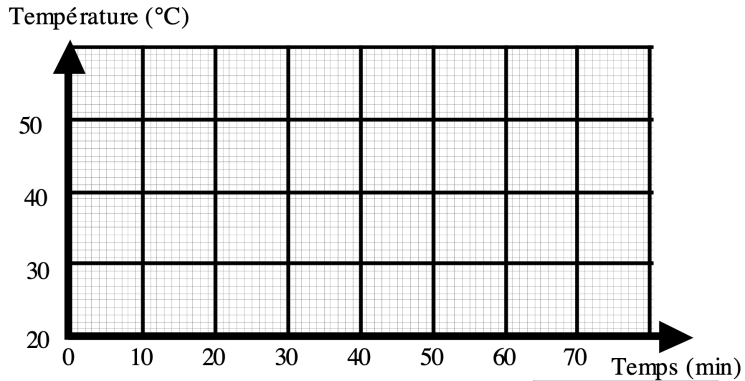
2-5 En utilisant vos données, tracez un graphique ( Evolution de la température en fonction du temps )
2-6 Légender votre graphique. Décrire l'évolution de la température...
Bonus : Est ce que le thermonmétre peut exploser lorqu'on le plonge dans de l'eau bouillante
2-7 Exercices
2-8 Exercices
On étudie la vaporisation d'un liquide inconnu.
Voici les valeurs que nous avons relevées. :
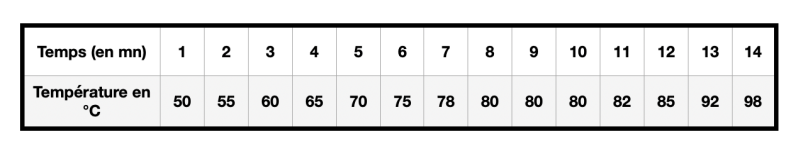
1-Trace l'évolution de la température du liquide au cours du temps
échelle : 1 cm <-> 1mn ; 1 cm <-> 10°C
2- a Observe-tu un changement d'état, si oui quelle est la durée ?
2- b Quel nom donne-t-on à ce changement d'état?
3- À quelle température a lieu le changement d'état ?
4- Peut-on en conclure que c'est un corps pur ?
5- De quel liquide pourrait-il s'agir ?

3-1 Rédiger un protocole expérimental pour la pesée des ingrédients solides (semoule, chocolat ou sucre).
3-2 Rédiger un protocole expérimental pour mesurer le volume de lait du doc 1.

Plus ça chauffe , plus ça gaze
4-1 Que provoque l'apport d'énergie ?

Entrainement :
Exercice 1 : Lire une température

a. Quelle est la valeur d’une division sur chaque thermomètre ?
b. Quelles sont les températures indiquées ?
Exercice 2 : Choisir la bonne courbe

Quelle est la courbe qui représente les variations de température en fonction du temps, lors du chauffage de l’eau pure sous la pression atmosphérique normale ?Justifie ta réponse.
Exercice 3 :
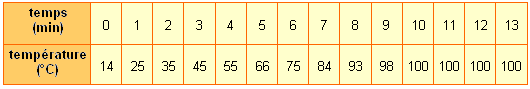
Lors de l’ étude de l’ ébullition de l’ eau, Mathias a tracé la courbe ci- dessous.

a. Quellegrandeur a-t-il porté sur l’axe des ordonnées ? Quelle est l’échelle choisie ?
b. Quelle grandeur a-t-il porté sur l’axe des abscisses ? Quelle est l’échelle choisie ?
c. Quelle est la température d’ébullition de l’eau ?
d. A quel instant l’eau a-t-elle commencé à bouillir ?
e. Quelle était la température de l’eau après trois minutes de chauffage ?
f. Peut-on prévoir la température à l’instant t=30 min ? Justifie ta réponse.
Exercice 4 : Graphique d’un changement
a. On place de l’éther pur (un liquide incolore autre que l’ eau) dans un becher que l’on place sur une plaque chauffante. Toutes les 5 minutes on note la température.
On place ces mesures dans un tableau.
Tracez le graphique de la température en fonction du temps sur votre cahier :

b. Quel est l’effet sur le liquide de la chaleur transmise par l’appareil de chauffage entre 0 min et 20 min ?
c. Entre 25 min et 45 min, comment varie la température ?
d. D’ après le graphique ou les mesures, que voit-on dans le liquide contenu dans le verre entre 25 min et 45 min (justifiez).
e. Faites le schéma de l’expérience entre 25 min et 45 min sans oublier les légendes (attention : le liquide de l’expérience n’est pas de l’eau mais de l’éther).
f. Entre 25 min et 45 min, l’appareil de chauffage chauffe-t-il l’éther ?
g. D’après le graphique ou les mesures, quelle est la température de vaporisation de l’éther ?
h. D’après le graphique ou les mesures, pourquoi est-on sûr que ce n’est pas de l’eau pure dont on a mesuré la température ?
Exercice 5 : Utiliser un tableau de donnée
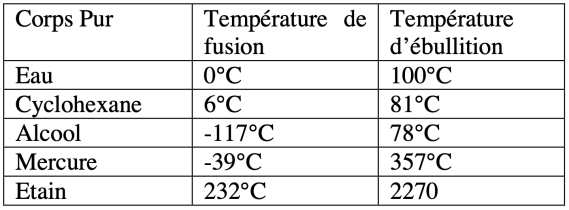
On désire connaître l’état physique de quelques corps purs pris à différentes températures. On dispose pour cela des données suivantes :

Indique, dans un tableau l'état physique du cyclohexane, de l’alcool et de l’étain aux températures suivantes : -55°C, -12°C, 60°C, 350°C.
Exercice 6 : le dioxygène
La température d’ébullition du dioxygène est de -183°C.
a. Dans quel état le trouve-t-on naturellement ?
b. A partir de quelle température le trouve-t-on à l’état liquide ?
c. Le dioxygène se trouve à l’état liquide dans certaines bouteilles. Comment est-ce possible ?

Construire un graphique
Lire un graphique
Placer des points niveau 2
